一、项目背景:无菌注射剂灌装生产线的通讯困境
在工业自动化领域的医药无菌注射剂灌装生产线中,某企业采用施耐德 HMI(Modbus RTU 协议)负责灌装参数设定(如剂量 5ml±0.02ml)、设备操作监控,搭配西门子 S7-1500 PLC(Modbus TCP 协议)控制灌装阀、无菌隔离舱、在线检漏设备的运行。两者需实时协同:HMI 需向 S7-1500 PLC 下发灌装剂量、灌装速度(100 瓶 / 分钟)、无菌舱压力设定值(0.12MPa),S7-1500 PLC 需反馈实际灌装剂量、设备运行状态、检漏结果(合格 / 不合格),以保障注射剂剂量精度与无菌安全。但因双方采用不同总线协议,缺乏直接通讯通道,原有 “操作员在 HMI 记录参数后手动录入 PLC” 的衔接方式效率低下,日均因参数偏差导致的生产停滞达 2 次,单次停滞需废弃整批药液(约 2000 瓶),直接损失超 12 万元。无菌注射剂生产作为医药行业的核心领域,是工业自动化中对无菌控制、剂量精度要求极高的前景行业(2025 年全球注射剂市场规模预计超 1800 亿美元),对工业物联网环境下数据的实时性、合规性提出了严苛标准(符合 GMP、FDA 21 CFR Part 11 要求)。
二、项目痛点
-
协议异构阻断灌装控制:HMI 的 Modbus RTU 协议与 S7-1500 PLC 的 Modbus TCP 协议无法直接兼容,无物联网网关中转时,灌装参数需操作员每 15 分钟在 HMI 记录后,通过 PLC 编程软件手动输入,单次数据传递延迟超 20 分钟,导致灌装剂量控制偏差超 0.05ml,曾引发 1 批注射剂剂量不合格,报废损失超 15 万元;生产节拍从 100 瓶 / 分钟降至 60 瓶 / 分钟,日产能从 12 万瓶降至 7.2 万瓶,效率下降 40%。
-
数据采集追溯断层:原有系统无专用数据采集器,灌装剂量、无菌舱压力、检漏合格率等关键工艺数据仅分别存储于 HMI 本地(存储周期 24 小时)与 PLC 内存,无法自动上传至工业物联网平台与 GMP 数据归档系统,审计追踪时需人工整理纸质记录,耗时超 60 小时,不符合 FDA 21 CFR Part 11 对 “电子数据不可篡改、可追溯” 的要求,面临监管部门整改风险。
-
工业环境适应性差:生产线位于无菌洁净区(Class 100),传统 RS485 转以太网模块防护等级低(IP20)、不耐受洁净区的湿热灭菌(温度 121℃、湿度 100%),日均通讯中断 1-2 次,每次中断需停产消毒并重启设备,恢复耗时超 4 小时,单日减少有效生产时间约 8 小时,损失产能超 4.8 万瓶。
-
设备负载超限引发安全风险:尝试通过第三方软件实现数据转发,导致 HMI 触控响应延迟超 3 秒(CPU 负载升至 89%)、S7-1500 PLC CPU 负载达 85%,超出安全运行阈值(HMI≤80%、PLC≤75%),引发灌装阀开关延迟,导致部分瓶体漏液,漏液率从 0.1% 升至 0.8%,额外增加清洁与物料损失成本超 6 万元 / 月。
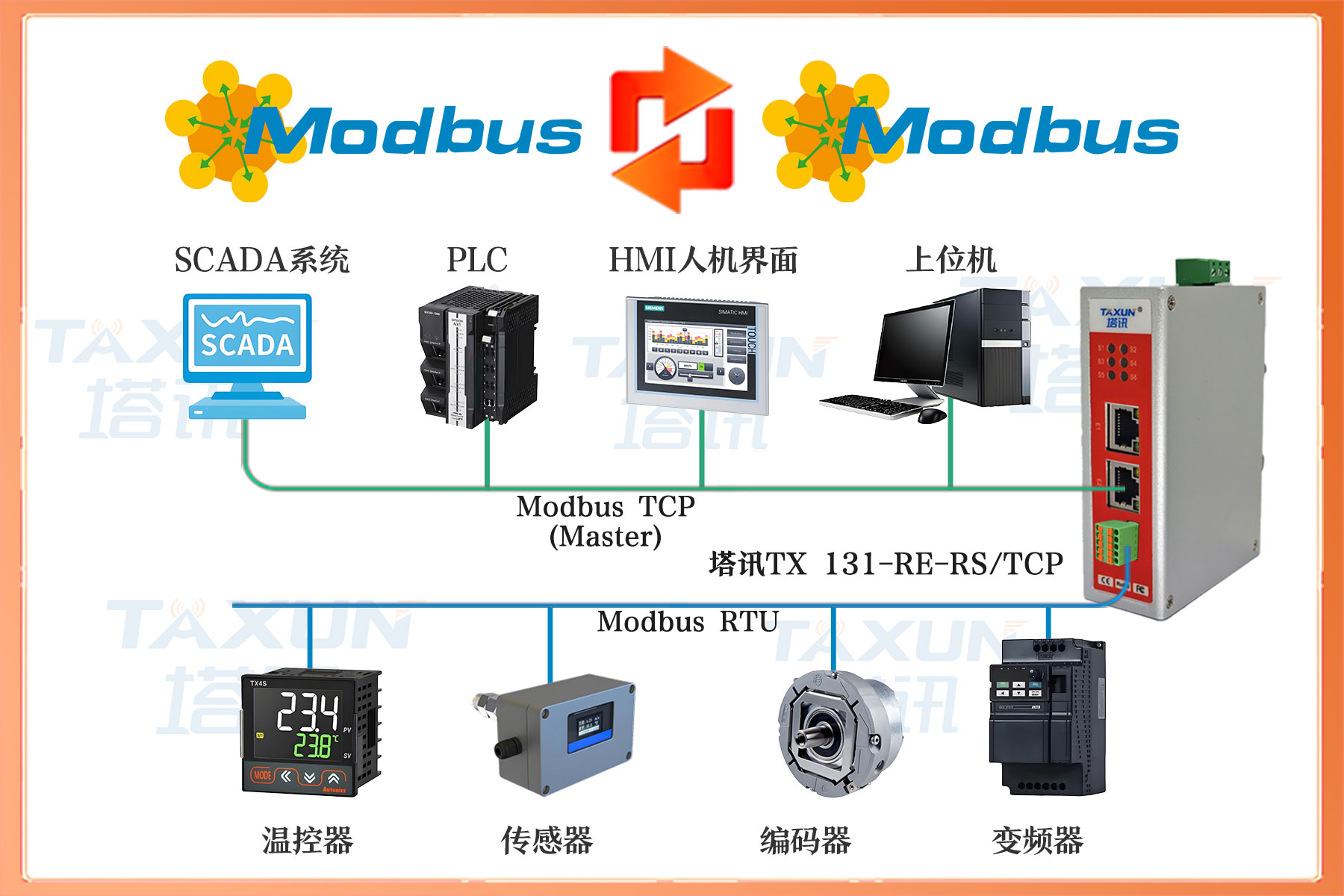
三、系统结构拓扑图

四、塔讯 TX 131-RE-RS/TCP 网关功能简介
作为核心工业网关,该设备实现 Modbus RTU 从站到 Modbus TCP 从站的双向协议转换,关键功能深度适配无菌注射剂灌装场景需求:
· 协议兼容:严格遵循 Modbus RTU(IEC 61158)与 Modbus TCP(IEC 61158)协议规范,支持 9600-115200bps 可调波特率(适配 HMI 通讯参数:9600bps、偶校验、8 数据位、1 停止位)与 10/100Mbps 自适应以太网速率,自动识别 S7-1500 PLC 的寄存器地址映射规则,确保灌装参数与指令传输无格式偏差,符合注射剂 “剂量零误差” 要求。
· 数据处理:内置双核工业级处理器,每秒可完成 2300 次以上数据转换,转换延迟≤21μs,支持 1800 点数据映射,满足灌装剂量(4 字节浮点数)、无菌舱压力(4 字节浮点数)、检漏结果(1 字节布尔值)等多类型数据同步传输,数据更新频率达 2 次 / 秒,符合 GMP 对 “实时监控” 的标准。
· 工业适配:具备 IP40 防护等级(适配洁净区环境),外壳采用 316L 不锈钢材质(耐湿热灭菌、耐腐蚀),支持 24VDC 宽压供电(±10% 波动兼容);采用宽温设计(10℃-50℃),耐受洁净区温湿度波动;抗电磁干扰性能符合 EN 61000-6-2 标准,避免检漏设备高频信号导致的数据丢包。
· 物联与合规扩展:支持本地数据缓存(容量 3GB,缓存周期 90 天),通过 MQTT 协议对接工业物联网平台与 GMP 数据服务器,实现工艺数据实时归档与不可篡改存储;内置审计追踪日志功能,记录每一次参数修改、数据传输的时间戳与操作员信息,满足 FDA 21 CFR Part 11 要求;支持故障自恢复,通讯中断后≤80ms 重新建立连接,保障无菌生产连续。

五、解决方案与实施过程
(一)方案设计
采用塔讯智能网关构建 “HMI - 网关 - PLC” 通讯架构:网关 Modbus RTU 侧作为 HMI 的从站,实时采集灌装剂量(DB1.DBD10)、灌装速度(DB1.DBD20)、无菌舱压力设定值(DB1.DBD30);Modbus TCP 侧作为 S7-1500 PLC 的从站,将采集到的参数传输至 PLC,同时接收 PLC 反馈的实际剂量(DB2.DBD10)、设备状态(M10.0-M10.2)、检漏结果(DB2.DBD20),实现双向数据实时交互,数据更新频率 2 次 / 秒,满足注射剂灌装控制需求。
(二)实施步骤
-
硬件部署:网关安装于洁净区外的控制室机柜内,通过耐灭菌屏蔽 RS485 电缆(长度 30 米,穿墙接线盒密封处理)接入 HMI 的 RS485 通讯端口;通过单模光纤(抗干扰性强,适配洁净区与控制室 400 米距离)连接 S7-1500 PLC 的以太网交换机,配置 IP 地址(192.168.11.100)与 PLC(192.168.11.10)同网段,做好独立接地处理(接地电阻≤4Ω),避免车间静电干扰。
-
参数配置:使用塔讯配置软件建立数据映射表 —— 将 HMI 的灌装参数(剂量:40001、速度:40002、压力:40003)映射至网关寄存器;将 PLC 的反馈数据(实际剂量:30001、设备状态:10001-10003、检漏结果:30002)映射至网关对应寄存器,设置数据更新周期 100ms,启用 “数据校验”“审计日志”“断网重连” 功能,日志保存周期 90 天。
-
联调与合规测试:在工业物联网平台与 HMI 同步验证数据传输(延迟≤21μs,丢包率 0%);模拟灌装剂量调整(从 5ml 降至 2ml),测试 PLC 接收指令后灌装阀的响应时间(≤50ms);邀请第三方机构验证审计日志符合 FDA 21 CFR Part 11 要求,确保通过 GMP 复评。

六、应用效果与前后对比
(一)实施后效果
-
灌装精度与合规性双提升:数据传输延迟降至 21μs 内,HMI 与 PLC 参数同步无偏差,灌装剂量控制偏差从 ±0.05ml 降至 ±0.01ml,剂量不合格事件从 2 次 / 日降至 0 次,每月减少产品废弃损失超 36 万元;生产节拍从 60 瓶 / 分钟提升至 110 瓶 / 分钟,日产能从 7.2 万瓶增至 13.2 万瓶,效率提升 83%,满足市场对注射剂的激增需求。
-
数据追溯效率大幅提升:通过网关将工艺数据自动归档至工业物联网平台与 GMP 服务器,审计追踪时间从 60 小时缩短至 12 分钟,顺利通过 FDA 现场检查;数据不可篡改功能保障电子数据合规,未再出现监管整改风险。
-
通讯稳定性适配洁净区环境:网关 IP40 防护与耐灭菌设计适配洁净区工况,连续运行 3 个月无通讯中断,设备故障率从 9% 降至 0.3%,停产恢复时间从 4 小时缩短至 15 分钟,单日增加有效生产时间 8 小时,月增产能超 38.4 万瓶。
-
设备负载与安全风险降低:HMI 触控响应延迟从 3 秒降至 0.1 秒(CPU 负载从 89% 降至 41%),S7-1500 PLC CPU 负载从 85% 降至 37%,均低于安全阈值;灌装阀开关延迟消除,漏液率从 0.8% 降至 0.05%,每年减少清洁与物料损失成本超 72 万元。

(二)效果对比表
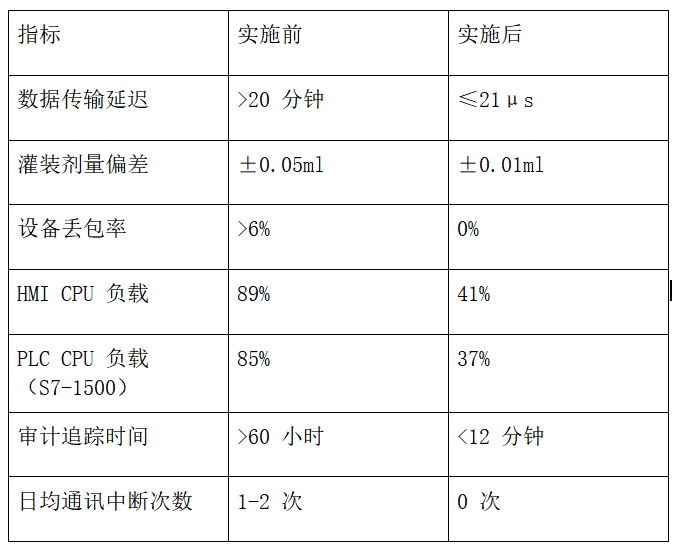
七、行业价值与后续扩展
本案例聚焦无菌注射剂灌装行业,该行业关乎患者用药安全,对生产过程的精度与合规性要求极高。此方案可复制至疫苗灌装、生物制剂灌装等场景,后续可扩展接入 MES 系统,实现灌装数据与生产订单、质量检测数据联动;或对接 AI 视觉检测系统,通过工业物联网平台分析灌装瓶体外观数据,自动识别瑕疵品,进一步提升注射剂生产的安全性与效率,助力企业满足全球严苛的医药监管标准。

![洛谷 B4413:[GESP202509 三级] 数组清零](http://pic.xiahunao.cn/洛谷 B4413:[GESP202509 三级] 数组清零)
 : 构建3G RNC端到端性能可观测性体系 - 指南)






)
)








